
Chimie Bioorganique et Bioinorganique

1.3. Synthèse et évaluation d'inhibiteurs d'aldose-cétose isomérases : aspects structuraux, mécanistiques et thérapeutiques
Objectifs :
Etude des aspects structuraux, mécanistiques et thérapeutiques des aldose-cétose isomérases :
- PGI : Phosphoglucose isomérases
- PMI : Phosphomannose isomérases
- PRI : Phosphoriboses isomérases
Stratégie :
- Synthèse et évaluation cinétique d'inhibiteurs compétitifs analogues d'intermédiaire de haute énergie (IHE) ou de l'état de transition (ET)
- Inhibiteurs monosaccharidiques phosphorylés de type : acide hydroxamique, hydrazide, amide, amine...
- Elaboration d'inhibiteurs "phosphomimes"
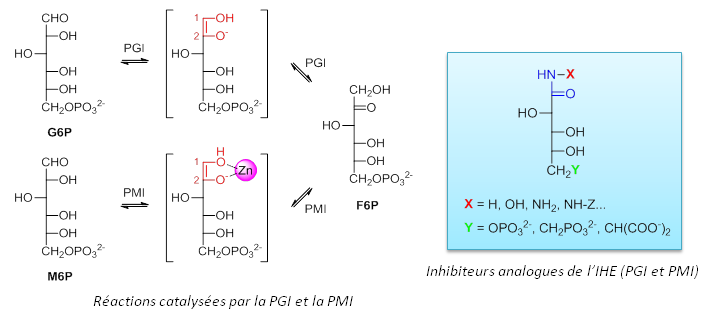
Résultats :
Collaborations :
|

